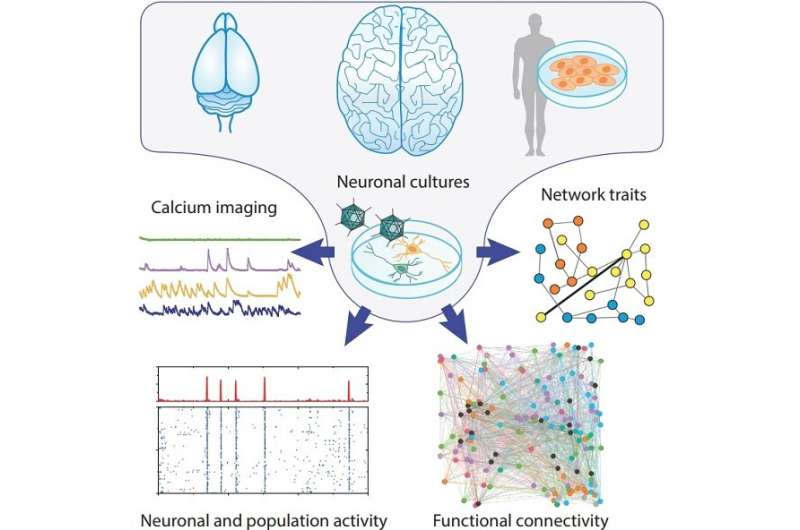
Generación de redes neuronales similares a las humanas a través de la reprogramación celular
estribillo gráfico. crédito: Informes de células madre (2022). DOI: 10.1016/j.stemcr.2022.11.014
Un estudio publicado en la revista Informes de células madre Él revela que la metodología de reprogramación celular permite la creación de redes neuronales que reproducen propiedades únicas de las células humanas -diferentes a las obtenidas de las células de roedores- con una dinámica temporal similar al desarrollo del cerebro humano.
Por lo tanto, los modelos celulares se basan en reprogramarlos células humanas Podría promover el desarrollo de nuevas terapias eficaces en la lucha contra las neuropatías y, al mismo tiempo, reducir el uso de experimentos con animales en el laboratorio.
El estudio ha sido liderado por el investigador Daniel Tornero Prieto, de la Facultad de Medicina y Ciencias de la Salud, el Instituto de Neurociencias de la UB (UBNeuro) y el IDIBAPS. En el estudio también han participado los investigadores Jordi Soriano Fradera y Estefanía Estévez-Priego, de la Facultad de Física y el Instituto de Sistemas Complejos de la UB (UBICS) y Zaal Kokia, de la Universidad de Lund (Suecia), entre otros.
Reprogramación celular para superar las limitaciones de los modelos animales
Aunque gran parte de nuestro genoma se comparte con la mayoría de los mamíferos, “existen diferencias significativas entre nuestras células y las de otras especies, como los roedores, que se utilizan como modelos animales para la mayoría de las enfermedades”, señala Daniel Tornero, MD, del Departamento de Biomedicina. en la Universidad de Buffalo.
“En particular, hay diferencias muy grandes en el cerebro, particularmente en términos de organización y conectividad. Esto hace que nuestras capacidades cognitivas sean muy diferentes y también explica por qué los defectos que dan lugar a enfermedades que afectan a nuestro cerebro no se reproducen de la misma manera”. en el cerebro de estos animales”.
Las limitaciones de los estudios en modelos animales pueden superarse con una técnica de reprogramación celular, basada en la inducción de células madre pluripotentes humanas (hiPSCs), método desarrollado por Shinya Yamanaka en 2007. Se trata de una metodología que puede generar cultivos de cualquier tipo celular a partir de las células de un adulto – Relativamente simple, efectivo y sin consideraciones éticas relevantes – Con gran potencial para Aplicacion clinica en Terapia Celular y Medicina Regenerativa.
Como parte del estudio, el equipo aplicó la técnica de registros del nivel de calcio intracelular para comparar las propiedades de los cultivos neuronales generados por la técnica de reprogramación celular a partir de células humanas con los obtenidos de roedores y cerebros humanos. Esta técnica proporciona una medida indirecta de la actividad neuronal: durante un impulso nervioso, que se transmite de una neurona a otra, los niveles de calcio aumentan de forma característica y pueden ser registrados por sensores de calcio intracelulares.
Este sistema de estudio permite el seguimiento de alta resolución de la actividad neuronal de forma dinámica a lo largo de la vida de un cultivo. La estrategia experimental se complementa con el uso de placas especiales que permiten rastrear un mismo grupo de células mediante marcadores incrustados en la superficie del cultivo, técnica que reduce variables y genera resultados más confiables y valiosos para el estudio de redes neuronales.
Diferencias entre diferentes circuitos neuronales
Por primera vez, el equipo pudo estudiar y caracterizar las propiedades de los diferentes circuitos neuronales generados, estructuras biológicas que a primera vista podrían parecer idénticas.
Los resultados muestran que las neuronas de origen humano se comportan de forma diferente a la hora de generar circuitos neuronales desde un punto de vista funcional. Estas propiedades pueden explicar en parte los problemas asociados con los modelos animales utilizados para estudiar enfermedades del cerebro humano.
“En primer lugar, lo que más nos llama la atención es la escala de tiempo que define la formación y maduración de una red neuronal. Los cultivos derivados de células humanas muestran un comportamiento dinámico rico y progresivo, de tal manera que se observa claramente el proceso de maduración de la red neuronal generada”. de 20 días a 45 días de cultivo”, dice Daniel Tornero. “Durante este período, gracias a los diversos descriptores que hemos desarrollado, hemos podido analizar cómo la red neuronal se vuelve más compleja con el tiempo, a medida que las neuronas humanas se vuelven más interconectadas”, agrega el investigador.
Además, las neuronas humanas son capaces de hacer conexiones mucho más largas dentro de la cultura, una propiedad determinada por su biología, ya que el cerebro humano es mucho más grande que el de los roedores.
“Sin embargo, los circuitos neuronales generados a partir de células de roedores exhiben un comportamiento monótono durante períodos muy cortos, con pocos cambios a lo largo de su desarrollo”, dice Tornero.
Protocolos seguros y bancos de células compatibles
Los modelos celulares basados en células humanas reprogramadas están emergiendo como un paso intermedio relevante entre los estudios en animales y la aplicación clínica. La generación de estos modelos celulares para el estudio de enfermedades a partir de células humanas reprogramadas está consolidada en estudios preclínicos -cultivos 2D o sistemas organ-on-a-chip (OoCs)- y, más recientemente, en la generación de sistemas 3D basados en sobre el uso de biomateriales, organoides o bioimpresión.
En medicina regenerativa, la aplicación de esta tecnología en estrategias de terapia celular presenta un gran potencial y existen numerosos ensayos clínicos sobre diversas enfermedades (diabetes tipo 1, infarto de miocardio, lesión medular, degeneración macular, enfermedad de Parkinson, etc.). Establecer protocolos seguros y fiables y establecer bancos de células compatibles con los diferentes grupos alogénicos presentes en la población son algunos de los retos más ambiciosos en este campo de estudio.
“Estos nuevos enfoques pueden ser muy valiosos para la validación de diferentes terapias preclínicas, especialmente cuando se estudian enfermedades que afectan a procesos complejos basados en la organización de circuitos neuronales (enfermedades del neurodesarrollo, trastorno del espectro autista, enfermedades neurodegenerativas, etc.)”, afirma Daniel Tornero. . hasta entonces”.
“Además, la reprogramación de células a partir de la inducción de células madre pluripotentes humanas permitirá crear modelos específicos de pacientes y utilizando herramientas de edición de genes (como la tecnología CRISPR/Cas9) se podrá obtener el control células Se corrige la mutación que causa la enfermedad”.
más información:
Estefanía Estévez-Priego et al, Las imágenes de calcio a largo plazo revelan un desarrollo funcional en cultivos derivados de hiPSC que son comparables a los cultivos primarios humanos pero no a los ratones, Informes de células madre (2022). DOI: 10.1016/j.stemcr.2022.11.014
Introducción de
Universidad de Barcelona
La frase: Obtenido el 22 de diciembre de 2022 de https://phys.org/news/2022-12-generating-human-like-neural-networks-cellular.html Generación de redes neuronales similares a las humanas a través de la reprogramación celular (22 de diciembre de 2022)
Este documento está sujeto a derechos de autor. Aparte de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin permiso por escrito. El contenido se proporciona únicamente con fines informativos.

“Defensor de la Web. Geek de la comida galardonado. Incapaz de escribir con guantes de boxeo puestos. Apasionado jugador”.