Los científicos han descubierto un nuevo sistema de edición de ADN en animales, capturado de bacterias hace más de 60 millones de años.
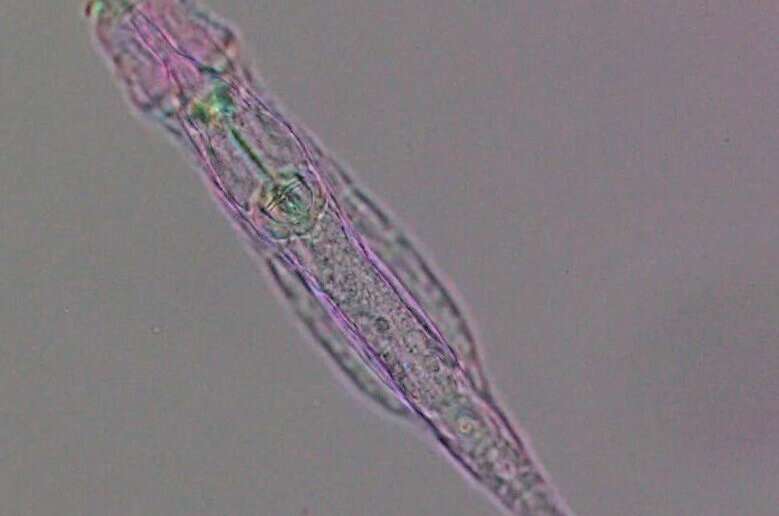
Rotífero bdelloide (Adineta vaga) bajo un microscopio polarizador multicolor. Crédito: M. Shrepak y E. Yoshnova
Su ADN contiene el modelo para construir su cuerpo, pero es un documento vivo: se pueden realizar modificaciones en el diseño a través de marcas epigenéticas.
Las marcas epigenéticas son modificaciones en las bases del ADN que no cambian el código genético básico, pero “escriben” información adicional encima que se puede heredar con su genoma. Por lo general, las marcas epigenéticas están reguladas la expresion genicagirar genes Encender o apagar – especialmente durante desarrollo temprano O cuando tu cuerpo está bajo estrés. También pueden suprimir los “genes saltadores”, elementos transponibles que amenazan la integridad de su genoma.
En humanos y otros eucariotas, se conocen dos signos principales de herencia epigenética. Un equipo del Laboratorio de Biología Marina (MBL) ha descubierto un tercer marcador genético nuevo, uno conocido anteriormente solo en bacterias, en rotíferos, bdeloides y pequeños animales de agua dulce. Este descubrimiento fundamental y sorprendente se informó esta semana en Comunicaciones de la naturaleza.
“Descubrimos en 2008 que los rotíferos son muy buenos para detectar genes extraños”, dijo la autora principal Irina Arkypova, científica en jefe del Josephine Bay Pole Center de MBL. “Lo que encontramos aquí es que los rotores, hace unos 60 millones de años, recogieron accidentalmente un gen bacteriano que les permitió introducir una nueva marca epigenética que antes no existía. “Esta es la primera vez que se demuestra que un gen transferido horizontalmente remodela el gen Sistema regulatorio en eucariotas.
“Esto es muy inusual y no se ha informado antes”, dijo Arkypova. “Se cree que los genes transferidos horizontalmente son preferentemente genes operativos, no genes reguladores. Es difícil imaginar cómo un solo gen transferido horizontalmente podría formar un nuevo sistema regulador, porque los sistemas reguladores actuales ya son muy complejos”.
“Es casi increíble”, dijo la coautora Irina Yushinova, científica investigadora en el laboratorio de Arkhipova. “Solo trata de imaginar, en algún momento, que un trozo de ADN bacteriano se ha fusionado en un trozo de ADN eucariótico. Y ambos se unieron rotíferosgenomas y formaron una enzima funcional. Esto no es fácil, incluso en el laboratorio, y ha ocurrido de forma natural. Luego, esta enzima sintetizada creó este asombroso sistema regulador, y los rotores de bdelloides pudieron comenzar a usarlo para controlar todos estos transposones saltadores. Es como magia”.
“No quieres que los transposones salten directamente a tu genoma”, dijo el primer autor Fernando Rodríguez, quien también es científico investigador en el laboratorio de Arkhipova. “Van a estropear las cosas, por lo que desea mantenerlos bajo control. Y el sistema epigenético para lograrlo es diferente en diferentes animales. En este caso, transferencia horizontal de genes De bacterias a rotíferos alineados Creó un nuevo sistema genético en animales que no había sido descrito antes”.
“Los rotíferos bdelloides, en particular, deberían mantener a raya a los vectores porque se reproducen asexualmente”, dijo Arkhipova. “Las cepas asexuales tienen menos medios para suprimir la reproducción de transposones dañinos, por lo que agregar una capa adicional de protección puede prevenir la ruptura mutacional. De hecho, el contenido de transposones es mucho más bajo en los bdelloides que en los eucariotas sexuales que no tienen esta capa epigenética adicional. en su sistema de defensa genómico”.
En las dos marcas epigenéticas previamente conocidas en eucariotas, una grupo metilo A la base de ADN se le añade citosina o adenina. La etiqueta recién descubierta por el equipo también es una modificación de la citosina, pero con un entorno bacteriano distinto para el grupo metilo, un resumen esencial de los eventos evolutivos que ocurrieron hace más de dos mil millones de años, cuando era marcas epigenéticas Aparecieron en los primeros eucariotas.
Los rotíferos bdelloides son animales muy resistentes, como han descubierto a lo largo de los años el laboratorio de Arkhipova y David Mark Welch en MBL. Pueden secarse por completo (secarse) durante semanas o meses seguidos y luego volver a la vida cuando hay agua disponible. Durante las fases secas, su ADN se divide en muchas partes. “Cuando los rehidratas o haces accesibles sus extremos de ADN, esta podría ser una oportunidad para que fragmentos de ADN extraños de bacterias, hongos o microalgas ingeridos se muevan hacia el genoma del rotífero”, dijo Arkhipova. Descubrieron que alrededor del 10 por ciento del genoma del rotífero proviene de fuentes que no son metazoos.
Sin embargo, el laboratorio de Arkhipova se sorprendió al encontrar un gen en el genoma del rotífero que se parece a una transferencia de metilo bacteriana (el transportador de metilo cataliza la transferencia de un grupo metilo al ADN). “Presumimos que este gen confiere esta nueva función de reprimir los transposones, y hemos pasado los últimos seis años probándolo”, dijo Arkhipova.
Es pronto para conocer las implicaciones del descubrimiento de este nuevo sistema epigenético en rotíferos. “Una buena comparación es el sistema CRISPR-Cas en bacterias, que comenzó como un descubrimiento de investigación básica. Ahora, CRISPR-Cas9 se usa de forma generalizada como una herramienta para la edición de genes en otros organismos”, dijo Rodríguez. “Este es un sistema nuevo. ¿Tendrá aplicaciones e implicaciones para futuras investigaciones? Es difícil saberlo”.
Estos descubrimientos abren la puerta a nuevas herramientas y direcciones de investigación para la investigación. genoma La funcionalidad y flexibilidad de este sistema de rotíferos. En el futuro, dicho conocimiento puede aplicarse de manera creativa para influir en la sociedad durante este tiempo de rápido cambio ambiental.
N4-metilcitosina bacteriana como marca epigenética en el ADN eucariótico. Comunicaciones de la naturaleza (2022).
Introducción de
laboratorio de biologia marina
La frase: Los científicos descubren un nuevo sistema de edición de ADN en animales, capturado de bacterias durante 60 años (28 de febrero de 2022) Obtenido el 28 de febrero de 2022 de https://phys.org/news/2022-02-scientists-dna-modification-animals- capturar. html
Este documento está sujeto a derechos de autor. Sin perjuicio de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin permiso por escrito. El contenido se proporciona únicamente con fines informativos.

“Defensor de la Web. Geek de la comida galardonado. Incapaz de escribir con guantes de boxeo puestos. Apasionado jugador”.